治療用アプタマーはどこに?

2022年8月4日 掲載
アプタマーを標的薬剤として使用する新たなアプローチは、将来的により広範な臨床使用への扉を開くかもしれません。
アプタマーは高い熱安定性、事実上あらゆる標的としっかりと結合する能力、容易かつスケーラブルな生産、バッチ間の均一性など1治療薬として多くの潜在的な利点を有しているにもかかわらず、臨床ではほとんど成功をおさめていません。腎クリアランスが速く、またヌクレアーゼに対する感受性が高いことに加えて、in vitroの精製成分に対するアプタマーのパフォーマンスが、必ずしもin vivoでの同様のパフォーマンスに繋がるとは限りません2。
しかし、アプタマーをより大規模な治療薬の標的成分として活用しようという最近の取り組みにより、これらの有望な分子が臨床でその潜在能力をフルに発揮する日がついに来るかもしれません。このブログ記事では治療法開発におけるアプタマーの最近の応用例をいくつか紹介します。近い将来、これらのイノベーションが市場に投入され、ヒトの健康が増進されることを期待しています。
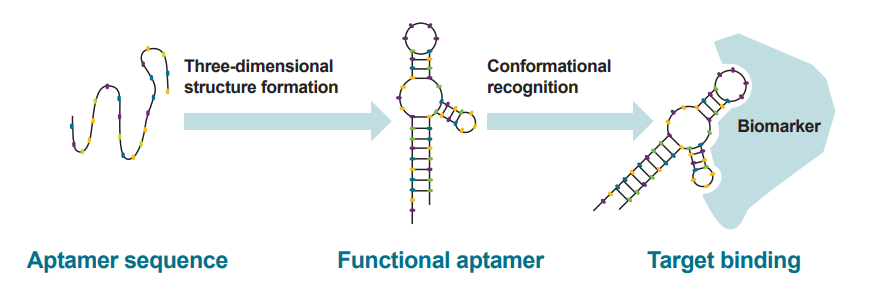
アプタマーとナノ粒子が培養細胞や小動物モデルで光線力学的療法(Photodynamic therapies, PDT)をもたらす
光線力学的療法と光熱療法(PDTとPTT)はがん治療のための有望なアプローチであり5、今日すでにいくつかの適応症に使用されています6, 7。PDTがうまく機能すれば、アポトーシスを誘導して腫瘍細胞を殺すことができます。しかしPDTはそれ自体の成功が問題となります。第一世代のアプローチの多くは腫瘍微小環境(TME)内に低酸素状態を作り出す一重項酸素(1O2)を発生させる光増感剤を使用します。少数の腫瘍細胞を死滅させる最初のアポトーシス反応が存在する可能性がありますが、低酸素状態は血管新生と腫瘍増殖を促進する保護シグナル伝達カスケードを活性化し、PDTを克服します。
PTTのような新しいアプローチは一重項酸素ではなく熱を発生する光増感剤を使用することで低酸素の問題を克服しようとしています。
腫瘍細胞の殺傷の様式にかかわらず、多くのチームが増感剤を腫瘍部位に局在化させる標的シグナルを加えることによって、PDTとPTTの両方の療法をより安全なものにしようとしています。ナノ粒子足場上で光増感剤と腫瘍細胞特異的アプタマーを組み合わせることで、研究者らは細胞および、動物モデルで有望な活性を示す標的化PDTおよびPTTを作製しています8-10。
ナノ液滴と脂質ナノ粒子上のアプタマーがsiRNA治療薬を送達する
商業化が遅れているもう一つの有望な治療法にsiRNAやmiRNAのような低分子RNAベースの医薬品があります。低分子RNAの明らかな課題は、治療効果が得られるまで血流中での持続時間を延長させることです。現在、脂質ナノ粒子やナノ液滴などのナノ材料が、送達のための手段として検討されています。新型コロナウイルス感染症(COVID-19)mRNAワクチンの送達に使用すると、驚くほど効果的であることがすでに示されています11。
ここで再びアプタマーが活躍し、標的送達のための選択的部位として機能します。
Guoら12は既に核酸ベースのphi29 DNAパッケージモーター(3WJ-pRNA)を用いており、治療薬としてsiRNAを送達しており、ターゲティングのためにRNAアプタマーを加えることで、治療薬の構築を簡略することができました。彼らは活性型siRNA、標的化アプタマー、3WJ-pRNAの足場といった、完全にRNAに基づく治療分子を創り出し、そして安定のためのナノ液滴に固定することができました。
別の例では、SARS-CoV-2スパイクタンパク質の受容体結合ドメイン(RBD)に特異的なアプタマーを用いて、SARS-CoV-2ヌクレオカプシドリン酸化タンパク質に対するRNAiを含む脂質ナノ粒子を標的化しました13。著者らはこの治療薬を重症のCOVID-19患者(36歳)にネブライザーで6日間投与し、CTスキャンおいて肺構造の改善を示すことができました。
アプタマーは治療用分子に直接添加されることもある
標的治療薬へのアプタマーの最後の応用例として、活性治療薬への直接の結合があります。最近の例はアプタマーをsiRNAに付加した腫瘍学的応用14や、アプタマーをトロンビンに付加した抗凝固応用15などがあります。
アプタマーのエキサイティングな未来
標的療法にアプタマーを組み込む論文が相次ぎ、また治療薬としてアプタマーの応用するための報告が続々と発表されており、LGC Biosearch Technologiesのチームは、そう遠くない未来にアプタマーが実用化された治療薬に応用されることを期待しています。
Biosearch Technologies社は、オリゴヌクレオチド修飾、固体担体および試薬の広範な製品ポートフォリオにより、お客様のアプタマーイノベーションを支援します。ロックド核酸や2’-F、2’-OMeホスホロアミダイトなど、オリゴの安定性やヌクレアーゼ耐性のための修飾があります。また2’-Fや2’-OMeおよびホスホロチオエート結合用の試薬も提供しています。オリゴヌクレオチド治療薬のツールボックスを是非ご覧ください。
参考文献
- Byun J. Recent Progress and Opportunities for Nucleic Acid Aptamers. Life. 2021;11(3):193. doi:10.3390/life11030193
- Yan AC, Levy M. Aptamer-Mediated Delivery and Cell-Targeting Aptamers: Room for Improvement. Nucleic Acid Ther. 2018;28(3):194-199. doi:10.1089/nat.2018.0732
- Nimjee SM, Rusconi CP, Sullenger BA. Aptamers: an emerging class of therapeutics, Annual Review of Medicine 2005;56, 555-583, doi:10.1146/annurev.med.56.062904.144915
- Sun H, et al. Oligonucleotide aptamers: new tools for targeted cancer therapy. Molecular Therapy Nucleic Acids 2014; 3, e182, doi:10.1038/mtna.2014.32
- Ji B, Wei M, Yang B. Recent advances in nanomedicines for photodynamic therapy (PDT)-driven cancer immunotherapy. Theranostics. 2022;12(1):434-458. doi:10.7150/thno.67300
- Photodynamic therapy (PDT). nhs.uk. Published October 19, 2017. Accessed May 1, 2022. https://www.nhs.uk/conditions/photodynamic-therapy/
- Photodynamic Therapy to Treat Cancer - National Cancer Institute. Published September 6, 2011. Accessed May 1, 2022. https://www.cancer.gov/about-cancer/treatment/types/photodynamic-therapy
- Li L, Zhou B, Xu H, Shi H, Gao L, Ge B. Zinc-Loaded Black Phosphorus Multifunctional Nanodelivery System Combined With Photothermal Therapy Have the Potential to Treat Prostate Cancer Patients Infected With COVID-19. Front Endocrinol. 2022;13:872411. doi:10.3389/fendo.2022.872411
- Chen L, Hong W, Duan S, Li Y, Wang J, Zhu J. Graphene quantum dots mediated magnetic chitosan drug delivery nanosystems for targeting synergistic photothermal-chemotherapy of hepatocellular carcinoma. Cancer Biol Ther. 2022;23(1):281-293. doi:10.1080/15384047.2022.2054249
- Ibarra LE, Camorani S, Agnello L, et al. Selective Photo-Assisted Eradication of Triple-Negative Breast Cancer Cells through Aptamer Decoration of Doped Conjugated Polymer Nanoparticles. Pharmaceutics. 2022;14(3):626. doi:10.3390/pharmaceutics14030626
- Lasting impact of lipid nanoparticles. Nat Rev Mater. 2021;6(12):1071-1071. doi:10.1038/s41578-021-00398-6
- Guo L, Shi D, Shang M, et al. Utilizing RNA nanotechnology to construct negatively charged and ultrasound-responsive nanodroplets for targeted delivery of siRNA. Drug Deliv. 2022;29(1):316-327. doi:10.1080/10717544.2022.2026532
- Saify Nabiabad H, Amini M, Demirdas S. Specific delivering of RNAi using Spike’s aptamer‐functionalized lipid nanoparticles for targeting SARS‐CoV‐2: A strong anti‐Covid drug in a clinical case study. Chem Biol Drug Des. Published online 2021. doi:10.1111/cbdd.13978
- Wei J, Song R, Sabbagh A, et al. Cell-directed aptamer therapeutic targeting for cancers including those within the central nervous system. Oncoimmunology. 2022;11(1):2062827. doi:10.1080/2162402X.2022.2062827
- Tsvetkov VB, Varizhuk IV, Kurochkin NN, et al. Anticoagulant Oligonucleotide–Peptide Conjugates: Identification of Thrombin Aptamer Conjugates with Improved Characteristics. Int J Mol Sci. 2022;23(7):3820. doi:10.3390/ijms23073820



